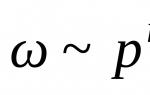Горение. Сгорание - органическое вещество Что образуется при горении органических веществ
Сгорание органических веществ сопровождается уменьшением внутренней энергии.
Сгорание органического вещества в избытке кислорода при 1000 - 1200 С проходит практически мгновенно, и нет необходимости опасаться того, что образовавшиеся пары воды и углекислый газ не успеют поглотиться в аппаратах. Поглотительная способность аскарита, безводного хлорида кальция и ангидрона весьма велики. Например, нами установлено, что органические вещества в количествах до 0 5 г сгорают количественно без катализаторов в струе кислорода, пропускаемого со скоростью 6 л / мин в течение 2 мин.
После сгорания органического вещества колбу вращают 1 мин.
Аппарат Сокслета. После сгорания органического вещества остаток в тигле прокаливают до постоянного веса. Для получения однородных результатов всю золу обычно переводят в сернокислые соли. Для этого к содержимому тигля прибавляют несколько капель концентрированной серной кислоты. Серную кислоту выпаривают под тягой на маленьком пламени газовой горелки и тигель прокаливают до постоянного веса.
Теплоты сгорания органических веществ довольно велики (обычно от 3 5 до 10 ккал / г), поэтому для их измерения часто используют жидкостные калориметры больших размеров - з калориметрический сосуд помещается от 2 до 4 л воды. Форма калориметрического сосуда и тип мешалки выбирают с учетом возможно быстрого и полного перемешивания всей массы жидкости.
Теплотой сгорания органического вещества называется тепловой эффект реакции полного сгорания данного вещества до СО2 (Газ), Н2ОЖИДК и соответствующих продуктов полного окисления других элементов, если они входили в состав данного вещества.
Продукты сгорания органического вещества вместе с содержащимся в нем в качестве примеси мышьяка массой 2 00 г были поглощены щелочным раствором ЬЬСЬ. Образовавшийся арсенат был оттитрован 15 85 мл 0 01 М Pb (NO3) 2 (/ С 0 9612) в присутствии пиридилазорезорцина.
Продукты сгорания органического вещества вместе с содержащимся в нем в качестве примеси мышьяка массой 2 00 г были поглощены щелочным раствором ШСЬ. Образовавшийся арсенат был оттитрован 15 85 мл 0 01 М Pb (NO3) 2 (/ (0 9612) в присутствии пиридилазорезорцина.
При сгорании органического вещества в калориметре выделяется тепло.
При сгорании органического вещества в водородном пламени образуется ряд ионизированных углеродных соединений. Вследствие образования этих ионов между изолированной горелкой, на которую подано напряжение, и электродом может протекать ток. Для изучения свойств пламенных детекторов разработана конструкция двухпламенного ионизационного детектора (рис. 1 и 2), который можно использовать и в виде однопламенного.
При сгорании органического вещества в водородном пламени образуется ряд ионизированных углеродных соединений. Вследствие образования этих ионов между изолированной горелкой, на которую подано напряжение, и электродом может протекать ток. Для изучения свойств пламенных детекторов разработана конструкция двухпламенного ионизационного детектора (рис. 1 и 2), который можно использовать и в виде одноплеменного.
Поэтому теплоту сгорания органических веществ (особенно многоатомных) можно считать относительно не изменяющейся с темпера-турой.
Измерение теплот сгорания органических веществ и изучение закономерностей в их величинах является одним из старейших разделов термохимии.
В продуктах сгорания органических веществ, содержащих азот, азот находится в свободном состоянии. Поэтому, чтобы открыть присутствие азота в органическом соединении, нужно разрушить это соединение и перевести азот в такое соединение, которое легко открыть какими-нибудь качественными реакциями.
Общий вид камерной цилиндрической вертикальной печи для сжигания сточных вод (конструкция ВНИИТ. На полноту сгорания органических веществ, находящихся в ПСВ-г, сильное влияние оказывают условия диспергирования и распределения жидкости форсунками в печи.
Определение теплоты сгорания органических веществ, производимое при помощи особых калориметрических установок в калориметрических бомбах, дает возможность вычислить энергию (теплоту) образования данных соединений, а отсюда и энергию отдельных химических связей.
Теплоты образования изомеров. Для теплот сгорания органических веществ еще не найдено общего выражения для всех отдельных закономерностей, наблюдаемых для разных классов органических соединений, но в пределах одного гомологического ряда имеются закономерности, весьма точно подтверждающиеся результатами опытов.
Схема прибора для определения органических веществ. Образующаяся при сгорании органических веществ двуокись углерода поглощается в барботере 10 титрованным раствором щелочи.
Анализ значений теплот сгорания органических веществ позволяет также делать выводы о стабильности их молекул.
Потеря, обусловленная сгоранием органического вещества, не поддается учету.
Так как при сгорании органического вещества выделяется двуокись серы и частично пары серного ангидрида, то процесс нужно вести под тягой. После сжигания смесь переносят в прибор (рис. 29), состоящий из круглодонной колбы, служащей для разложения аммонийных солей и отгонки аммиака, соединенной через каплеуловитель с холодильником. Нижний конец холодильника опущен в приемник с раствором кислоты.
Так, при сгорании органических веществ всегда образуется вода; она и должна быть признана элементарным телом.
Это осветление происходит вследствие сгорания органического вещества, в результате чего мета-морфизованные разности теряют свой характерный запах. Фосфориты эти имеют чаще всего тонкослоистую текстуру, пронизаны мелкими трещинами, становятся более хрупкими, иногда рассыпчатыми, мажущимися породами.
Качество сжигания или полноту сгорания органических веществ было решено контролировать по степени затемнен-ности дымовых газов.
В настоящее время по энтальпиям сгорания органических веществ накоплен очень обширный экспериментальный материал. Однако далеко не весь этот материал следует рассматривать как достаточно достоверный. Можно полностью согласиться с высказанным Россини еще в 1937 г. мнением о том, что все полученные до начала тридцатых годов нашего столетия числовые данные по энтальпиям сгорания органических веществ нельзя считать надежными, несмотря на то что во многих из выполненных в то время работ авторам удавалось достичь очень высокой воспроизводимости (до 0 03 - 0 05 %) результатов калориметрических измерений.
В нижнем пламени 17 происходит сгораний органических веществ, в том числе растворителя. В верхнем пламени 19 наблюдается эмиссия представляющих интерес молекул. Детектор более устойчив при вводе больших концентраций органических веществ.
Остаток, полученный в результате сгорания органического вещества, называется золой.
Накопление вполне надежных данных по энтальпиям сгорания органических веществ стало возможным только начиная с 30 - х годов нашего века.
Представляет собой продукт, получаемый при сгорании органических веществ без доступа воздуха; обладает большой поверхностью, ч го обусловливает его адсорбционную способность в отношении газов и многих растворенных веществ.
Пусть наша задача состоит в определении теплоты сгорания органического вещества. В этом случае, даже при наличии систематических ошибок в измерении подъема температуры в главном периоде, мы получим величину теплоты сгорания исследуемого вещества не искаженной.
Для измерения теплот реакций, особенно теплот сгорания органических веществ, используют прочный герметичный сосуд из нержавеющей стали - так называемую калориметрическую бомбу, в которой сжигают отвешенное количество вещества под давлением кислорода 20 - 40 атм. Вещество поджигают стальной проволокой, через которую пропускают электрический ток; при этом вещество испаряется.
Для количественного поглощения воды, образующейся при сгорании органического вещества, служит U-образная трубка (рис. 43), наполненная безводным зерне-ным хлористым кальцием, предварительно отсеянным от мелких частиц.
Наполненная хлоркальциевая трубка. Для количественного поглощения воды, образующейся при сгорании органического вещества, служит U-образная трубка (рис. 43), наполненная безводным зерненым хлористым кальцием, предварительно отсеянным от мелких частиц.
Для количественного поглощения воды, образующейся при сгорании органического вещества, служит U-образная трубка (рис. 43), наполненная безводным зерне-ньш хлористым кальцием, предварительно отсеянным от мелких частиц.
Графики изменения минерального состава грунтов в результате. В интервале температур 350 - 700 С происходит сгорание органических веществ, продукты окисления которых удаляются о аморфизации глинистых минералов.
В процессе биологического окисления замечательно то, что сгорание органического вещества за счет молекулярного кислорода, которое происходит с большой скоростью при невысокой температуре тела, осуществляется.
Накопленный в настоящее время термохимический материал по энтальпиям сгорания органических веществ и вычисленные на его основе величины стандартных энтальпий образования этих веществ дают возможность вычислить изменение энтальпии во многих реакциях. Однако следует иметь в виду, что даже при условии измерения энтальпий сгорания с очень высокой относительной точностью (например, 0 01 - 0 02 %) вычисленные из этих данных энтальпии соответствующих реакций часто могут быть получены лишь с очень большой величиной относительной погрешности. Погрешность особенно увеличивается в тех случаях, когда тепловой эффект реакции мал.
Наиболее точными измерениями в калориметрии являются определения теплоты сгорания органических веществ и теплоемкости.
Учащимся уже, известны причины образования копоти при сгорании органических веществ. Учитель предлагает им самим объяснить наблюдаемое явление.
Во второй главе книги сжато изложены вопросы измерения энтальпий сгорания органических веществ, содержащих помимо С, Н, О и другие элементы. Эта область калориметрии в настоящее время бурно развивается и совершенствуется.
Калориметрическая установка (калориметр) предназначена для определения теплоты сгорания органических веществ, в том числе углей.
В природе самопроизвольно совершаются медленные процессы, аналогичные как сгоранию органических веществ, полному или неполному, так и сухой перегонке. На поверхности земли при достаточном доступе воздуха остатки растений или животных подвергаются обычно сложным процессам гниения или тления под действием микроорганизмов. Окончательным результатом этих процессов является полное сгорание углерод - и водо-родсодержащих веществ с образованием двуокиси углерода и воды; азот частью выделяется в свободном виде или в виде а.
В природе самопроизвольно совершаются медленные процессы, аналогичные как сгоранию органических веществ, полному или неполному, так и сухой перегонке.
Сжигание необходимо производить под тягой, так как при сгорании органического вещества выделяется сернистый газ и частично пары серного ангидрида.
Следует отметить две основные причины несовершенства старых данных по энтальпиям сгорания органических веществ. Первая из них - это недостаточная степень чистоты объектов исследования. Во многих работах того времени сведения о чистоте исследованных веществ вообще отсутствуют.
ГОРЕНИЕ, сложный физико-химический процесс превращения вещества; развивается в режиме прогрессирующего самоускорения, связанного с лавинообразным накоплением в реагирующей системе тепловой энергии и активных промежуточных частиц - атомов, свободных радикалов и др. Горение используется в энергетике при производстве теплоты, работе транспорта, реактивных двигателей, а также в технологических процессах и осуществляется главным образом в камерах сгорания двигателей, топках, печах. С явлением горения человек имеет дело при пожарах, производстве и использовании взрывчатых веществ.
Развитие представлений о горении связано с именами М. Фарадея (горение свечи), М. В. Ломоносова (соединение веществ с кислородом), горения Шталя (теория флогистона), В. А. Михельсона (теория скорости распространения пламени) и др. В разработку современной теории горения значительный вклад внесли российские учёные Н. Н. Семёнов, Я. Б. Зельдович, Д. А. Франк-Каменецкий и др.
В большинстве случаев в основе горения лежит реакция окисления, в которой в качестве так называемого горючего могут участвовать почти все органические и многие неорганические вещества, в качестве окислителя - кислород, озон, галогены, перхлораты, нитросоединения и пр. Например, наибольшее практическое значение имеют процессы горения углеводородных горючих (природного горючего газа, нефти, углей, торфа и пр.) в присутствии кислорода. В режиме горения происходят также некоторые другие реакции (например, разложения, прямого синтеза из элементов).
В реальных условиях помимо продуктов полного сгорания, не способных к дальнейшему горению (диоксида углерода, воды и пр.), образуются другие химические соединения, называемые продуктами неполного горения, в том числе монооксид углерода, оксиды азота, серы, альдегиды, кислоты, бенз[а]пирен. Именно они обусловливают вредность и токсичность выбросов, загрязняют среду обитания и в итоге создают для современного общества экологические проблемы. Многие специалисты полагают, что за счёт процессов организованного горения, главным образом в энергетике, сопровождающихся образованием диоксида углерода и других парниковых газов, происходит потепление климата. К ухудшению качества среды обитания приводят также лесные и торфяные пожары, пожары на складах, химических предприятиях (в том числе использующих технологии хлорорганического синтеза), в местах добычи и переработки нефти и на других пожаро- и взрывоопасных объектах. Например, при горении трансформаторных жидкостей, твёрдых бытовых отходов, полимерных материалов на основе поливинилхлорида происходит образование диоксинов и других суперэкотоксикантов и загрязнение ими окружающей среды.
Основными характеристиками горения являются теплота сгорания горючего вещества, а также адиабатическая температура (температура, которая теоретически могла бы быть достигнута при полном сгорании вещества без потерь теплоты) и скорость процесса. Химические превращения при горении сопровождаются интенсивным тепло- и массообменом с окружающей средой и характеризуются соответствующими гидро- и газодинамическими закономерностями. При горении происходит излучение света в разных диапазонах длин волн, но, как правило, яркое свечение пламенем наблюдается в видимой области. Полное описание процесса горения можно провести с использованием закономерностей макрокинетики.
Важнейшая особенность процесса горения - способность к распространению в пространстве. Различают дефлаграционное и детонационное горение. В первом случае (дефлаграция) распространение горения осуществляется за счёт теплопроводности путём передачи теплоты от горящего объёма в соседние участки смеси, во втором - зажигание и распространение горения происходит за счёт сжатия вещества ударной волной (горение взрывчатых веществ). В свою очередь, дефлаграционное горение подразделяют на ламинарное и турбулентное.
Обычно линейная скорость горения выражается через скорость перемещения фронта реакции (пламени), массовая скорость горения - как количество горючего, сгорающего в единицу времени. Скорость горения зависит от природы и состава горючей смеси, давления и пр. Например, при ламинарном горении углеводородных воздушных смесей скорость распространения пламени составляет в среднем 0,4-0,8 м/с. Распространение пламени в турбулентном потоке газа приводит к искажению фронта горения, расширению зоны протекания химических реакций, а следовательно, к ускорению горения. На скорость горения влияют степень и масштабы турбулентности.
По агрегатному состоянию окислителя и горючего горение разделяют на гомогенное и гетерогенное. Примером гомогенного горения является горение пламенем горючих газов, паров керосина, бензина, спирта в воздухе. При гетерогенном горении (в том числе тлении - беспламенном горения) реакция происходит на поверхности раздела фаз газ - твёрдое тело (металлы, уголь). Если окислитель и горючее предварительно смешаны между собой, то гомогенное горения происходит в кинетическом режиме. Так как температура горения намного выше температуры кипения жидкостей и температуры возгонки некоторых твёрдых веществ, то их горение протекает в гомогенной смеси, а если горючее и окислитель заранее не смешаны, то в диффузионном режиме. Для газовых систем возможны как кинетический, так и диффузионный режимы горения. Определяющая роль разветвлённого цепного механизма процессов газофазного горения позволяет управлять этими процессами путём варьирования скоростей разветвления и обрыва цепей с помощью химически активных примесей.
Для любого вида горения характерны стадия воспламенения и последующий период устойчивого горения вещества с образованием продуктов полного и неполного горения. Различают два способа теплового воспламенения: самовоспламенение и зажигание. При самовоспламенении процесс происходит во всём объёме горючей смеси. При зажигании (вынужденном воспламенении) нагрев системы или накопление активных центров происходит вблизи источника зажигания (искра, пламя, нагретое тело). Температура воспламенения зависит от давления, состава горючего и прочих параметров и для большинства органических веществ находится в интервале 500-800 К.
Существуют критические предельные параметры горения, и вне этих пределов горения (как самопроизвольно протекающий процесс) невозможно. Этими параметрами для каждой горючей смеси являются соотношение объёмов горючего и окислителя, температура, давление, содержание примесей, в том числе концентрация в горючей смеси флегматизаторов (СО 2 , N 2 , Ar и др.) и ингибиторов (С 2 F 4 Br 2 , CH 2 CI 2 F 2 и др.), и пр. Для газов обычно указывают концентрационные, для жидкостей и твёрдых веществ - температурные пределы горения.
Выяснение законов горения и установление критических параметров воспламенения, развития и прекращения процесса горения - необходимое условие управления процессами горения, используемыми в различных сферах человеческой деятельности, обеспечения пожаро- и взрывобезопасности технологических процессов и объектов.
Лит.: Зельдович Я. Б. Теория горения и детонации газов. М.; Л., 1944; Иост В. Взрывы и горение в газах. М., 1952; Семенов Н. Н. О некоторых проблемах химической кинетики и реакционной способности. М., 1954; Хитрин Л. Н. Физика горения и взрыва. М., 1957; Кнорре Г. Ф. Топочные процессы. 2-е изд. М.; Л., 1959; Гейдон А. Г., Вольфгард Х. Пламя, его структура, излучение и температура. М., 1959; Вильямс Ф. А. Теория горения. М., 1971; Математическая теория горения и взрыва. М., 1980; Lewis В., Elbe G. von. Combustion, flames and explosions of gases. 3rd ed. Orlando, 1987; Франк-Каменецкий Д. А. Диффузия и теплопередача в химической кинетике. 3-е изд. М., 1987; Denisov Е. Т., Azatyan V. V. Inhibition of chain reactions. L., 2000; Исаева Л. К. Пожары и окружающая среда. М., 2001.
1.6. ПРОДУКТЫ ГОРЕНИЯ
Продукты горения – это газообразные, жидкие или твердые вещества, образующиеся в процессе горения. Состав продуктов сгорания зависит от состава горящего вещества и от условий его горения. Органические и неорганические горючие вещества состоят, главным образом, из углерода, кислорода, водорода, серы, фосфора и азота. Из них углерод, водород, сера и фосфор способны окисляться при температуре горения и образовывать продукты горения: СО, CO 2 , SO 2 , P 2 O 5 . Азот при температуре горения не окисляется и выделяется в свободном состоянии, а кислород расходуется на окисление горючих элементов вещества. Все указанные продукты сгорания (за исключение окиси углерода СО) гореть в дальнейшем больше не способны. Они образуются при полном сгорании, то есть при горении, которое протекает при доступе достаточного количества воздуха и при высокой температуре.
При неполном сгорании органических веществ в условиях низких температур и недостатка воздуха образуются более разнообразные продукты – окись углерода, спирты, кетоны, альдегиды, кислоты и другие сложные химические соединения. Они получаются при частичном окислении как самого горючего, так и продуктов его сухой перегонки (пиролиза). Эти продукты образуют едкий и ядовитый дым. Кроме того, продукты неполного горения сами способны гореть и образовывать с воздухом взрывчатые смеси. Такие взрывы бывают при тушении пожаров в подвалах, сушилках и в закрытых помещениях с большим количеством горючего материала. Рассмотрим кратко свойства основных продуктов горения.
Углекислый газ
Углекислый газ или двуокись углерода (СО 2) – продукт полного горения углерода. Не имеет запаха и цвета. Плотность его по отношению к воздуху = 1.52. Плотность углекислого газа при температуре Т = 0 0 С и при нормальном давлении р = 760 миллиметров ртутного столба (мм Hg ) равна 1.96 кг/м 3 (плотность воздуха при этих же условиях равна ρ = 1.29 кг/м 3). Углекислый газ хорошо растворим в воде (при Т = 15 0 С в одном литре воды растворяется один литр газа). Углекислый газ не поддерживает горение веществ, за исключением щелочных и щелочно-земельных металлов. Горение магния, например, происходит в атмосфере углекислого газа по уравнению:
CO 2 +2 Mg = C + 2 MgO .
Токсичность углекислого газа незначительна. Концентрация углекислого газа в воздухе 1.5% безвредна для человека длительное время. При концентрации углекислого газа в воздухе, превышающей 3-4.5%, нахождение в помещении и вдыхание газа в течение получаса опасно для жизни. При температуре Т = 0 0 С и давлении р = 3,6 МПа углекислый газ переходит в жидкое состояние. Температура кипения жидкой углекислоты составляет Т = –78 0 С. При быстром испарении жидкой углекислоты газ охлаждается и переходит в твердое состояние. Как в жидком, так и твердом состоянии, капли и порошки углекислоты применяются для тушения пожаров.
Оксид углерода
Оксид углерода или угарный газ (СО) – продукт неполного сгорания углерода. Этот газ не имеет запаха и цвета, поэтому особо опасен. Относительная плотность = 0.97. Плотность угарного газа при Т = 0 0 С и р = 760 мм Hg составляет 1.25 кг/м 3 . Этот газ легче воздуха и скапливается в верхней части помещения при пожарах. В воде оксид углерода почти не растворяется. Способен гореть и с воздухом образует взрывчатые смеси. Угарный газ при горении дает пламя синего цвета. Угарный газ является очень токсичным. Вдыхание воздуха с концентрацией угарного газа 0.4% смертельно для человека. Стандартные противогазы от угарного газа не защищают, поэтому при пожарах применяются специальные фильтры или кислородные изолирующие приборы.
Сернистый газ
Сернистый газ (SO 2 ) – продукт горения серы и сернистых соединений. Бесцветный газ с характерным резким запахом. Относительная плотность сернистого газа = 2.25. Плотность этого газа при Т = 0 0 С и р = 760 мм Hg составляет 2.9 кг/м 3 , то есть он намного тяжелее воздуха. Сернистый газ хорошо растворяется в воде, например, при температуре Т = 0 0 С в одном литре воды растворяется восемьдесят литров SO 2 , а при Т = 20 0 С – сорок литров. Сернистый газ горение не поддерживает. Действует раздражающим образом на слизистые оболочки дыхательных путей, вследствие чего является очень токсичным.
Дым
При горении многих веществ, кроме рассмотренных выше продуктов сгорания выделяется дым – дисперсная система, состоящая из мельчайших твердых частиц, находящихся во взвешенном состоянии в каком-либо газе. Диаметр частиц дыма составляет 10 -4 –10 -6 см (от 1 до 0.01 мкм). Отметим, что 1 мкм (микрон) равен 10 -6 м или 10 -4 см. Более крупные твердые частицы, образующиеся при горении, быстро оседают в виде копоти и сажи. При горении органических веществ дым содержит твердые частицы сажи, взвешенные в CO 2 , CO , N 2 , SO 2 и других газах. В зависимости от состава и условий горения вещества получаются различные по составу и по цвету дымы. При горении дерева, например, образуется серовато-черный дым, ткани – бурый дым, нефтепродуктов – черный дым, фосфора – белый дым, бумаги, соломы – беловато-желтый дым.
Скорость горения веществ и материалов в кислороде (жидком и газообразном) в 10-100 раз выше, чем на воздухе. Особенно велики скорости горения органических соединений.
В природе окись углерода содержится лишь в газах вулканов, рудников и болот. В промышленности окись углерода получают сухой перегонкой, а также газификацией углей. Кроме того, она образуется при горении органических соединений в условиях недостатка кислорода. Например, при полном сгорании метана образуется двуокись углерода
Примерное постоянство Тал, со объясняется следующим образом. Как было отмечено выше, горение органических соединений в воздухе протекает в две стадии. При этом лимитирую-
Состав продуктов сгорания зависит от состава горящего вещества, условий, в которых происходит горение, и главным образом полноты сгорания. В продуктах сгорания могут содержаться многие неорганические вещества (углерод, азот, водород, сера, фосфор и др.) и их окислы, а также спирты, кетоны, альдегиды и другие органические соединения. Образующийся в процессе горения дым состоит из мельчайших твердых частиц размером от 0,01 до
При умеренных температурах горения - обычно до 2000-2200° К для 1 ат (абс) - равновесный состав продуктов адиабатической реакции многих систем, состоящих из углерода, водорода, кислорода и азота, с хорошей точностью определяется простыми стехиометри-ческими соотношениями. Такие системы, образующиеся при сгорании смесей различных органических соединений с кислородом, - наиболее распространенный тип продуктов сгорания. При избытке
Специфическое действие ингибирующих добавок ограничено. Наиболее эффективны производные насыщенных углеводородов, у которых большая часть атомов водорода замещена атомами галоидов. Галоидпроизводные органических соединений, способные окисляться, затрудняют горение и уменьшают нормальную скорость пламени, по-видимому, только для смесей с избытком горючего. Добавление таких продуктов к бедным смесям может увеличивать скорость пламени вследствие возрастания при этом калорийности смеси .
Завершая обзор исследований в теории горения гетерогенных систем, посвященных выявлению роли радиации, отметим следующее. В литературе имеются экспериментальные доказательства существования радиационного механизма воспламенения аэрозолей некоторых металлов и углеродсодержащих соединений излучением горящих аэрозолей циркония и титана . Для ряда высокомолекулярных органических соединений, в том числе полимеров, можно наблюдать образование коксового остатка в процессе газификации вещества под действием внешнего излучения. Образующиеся высокоуглеродистые соединения в принципе могут явиться центрами зажигания в свежем аэрозоле. Оценки, однако, показывают, что практическая реализация схемы прогрева продукты горения - частицы свежей смеси ->- газификация с образованием кокса -> самовоспламенение летучих наступает при весьма широких фронтах пламени (диаметр канала составляет несколько метров), когда уже необходимо принимать во внимание газодинамические эффекты . Тем не менее энергетический баланс во фронте пламени при уточнении расчетных характеристик должен учитывать теплообмен радиацией (по оценкам Палмера доля радиации в теплообмене для систем различных масштабов меньше 20%), особенно для крупномасштабных процессов.
Процесс горения частиц полимеров, распределенных в воздухе, имеет много общего с горением аэрозолей других органических веществ. Под воздействием теплового потока от источника зажигания (при воспламенении) или от фронта пламени (при распространении фронта пламени) происходит прогрев частиц. Прогрев сопровождается процессом термоокислительной деструкции, в результате которой образуются низкомолекулярные газообразные продукты. В зоне пламени эти низкомолекулярные продукты сгорают до конечного состояния (в условиях, максимально благоприятствующих горению, - до СОг и Н20). Состав продуктов термоокислительной деструкции зависит от химического строения макромолекул полимера, условий зажигания и горения. В общем случае полимеры состоят из горючей и негорючей частей. Горючую часть составляют водород, оксид углерода, насыщенные и ненасыщенные низшие углеводороды, низшие альдегиды, кетоны, спирты и другие органические соединения. В негорючую часть входят пары воды, азот, диоксид углерода, галогеноводороды.
Энергию, используемую для расщепления, называют энергией разрыва связи. Она составляет 50-100 ккал-моль-1. При подводе малого количества энергии разрываются прежде всего ослабленные связи. В реакциях горения образование радикалов происходит почти исключительно за счет пиролиза. При пиролизе органических соединений могут возникнуть три случая
Образование. ПАУ образуются в результате пиролиза или неполного сгорания органического вещества, содержащего углерод и водород. При высоких температурах в результате пиролиза органических соединений образуются фрагменты молекул и радикалы, которые соединяются и образуют ПАУ. Состав конечного продукта пиролизного синтеза зависит от топлива, температуры и от времени прерывания в зоне горения. К топливу, после сгорания которого образуются ПАУ, относится метан, другие углеводороды, лигнины, пептиды, липиды и т.д. Тем не менее, соединения, содержащие разветвление цепи, ненасыщенные связи или циклические структуры, обычно благоприятствуют образованию ПАУ. Очевидно, ПАУ выделяются в виде паров из зоны горения. Из-за низкого давления пара большинство ПАУ мгновенно концентрируются на частичках сажи либо сами образуют мельчайшие частички. ПАУ, поступающие в атмосферу в виде пара, адсорбируются содержащимися в воздухе частицами. Содержащие ПАУ аэрозоли, таким образом распыляемые в воздухе, могут переноситься ветром на большие расстояния.
Распространение. Оксид углерода получается при сжигании органического материала типа угля, древесины, бумаги, масла, бензина, газа, взрывчатых веществ или карбонатных материалов любого другого типа в условиях недостатка воздуха или кислорода. Когда процесс горения происходит при избыточном питании воздухом и пламя не контактирует с какими-либо поверхностями, окись углерода не образуется. СО образуется в том случае, если пламя контактирует с поверхностью, температура которой ниже, чем температура воспламенения газообразной части пламени. Естественным путем образуется 90% атмосферного СО, а в результате деятельности человека производится 10%. На двигатели транспортных средств приходится от 55 до 60% всего количества СО искусственного происхождения. Выхлопной газ бензинового двигателя (электрическое зажигание) является обычным источником образования СО. Выхлопной газ дизельного двигателя (компрессионное воспламенение) содержит приблизительно 0,1 % СО, если двигатель работает надлежащим образом, однако неправильно отрегулированный, перегруженный или технически плохо обслуживаемый дизельный двигатель может выбрасывать значительные количества СО. Тепловые или каталитические дожигатели в выхлопных трубах значительно снижают количество СО. Другими основными источниками СО являются литейные производства, установки каталитического крекинга на нефтеперерабатывающих предприятиях, процессы дистилляции угля и древесины, известеобжигательные печи и печи восстановления на заводах крафт-бумаги, производство синтетического метанола и других органических соединений из оксида углерода, спекание загрузочного сырья доменной печи, производство карбида, производство формальдегида, заводы технического углерода, коксовые батареи, газовые предприятия и заводы по переработке отходов.
Концентрации примесей, которые возникают преимущественно из источников, связанных с процессом горения, подвержены чрезвычайно большим временным изменениям, а их выделение является прерывистым. Эпизодические выпуски летучих органических соединений благодаря человеческой активности, например рисованию или малярным работам, также приводят к большим временным вариациям в выделениях. Другие выделения, подобные выпуску в воздух помещений формальдегида изделиями из дерева, могут варьироваться в зависимости от температуры и колебаний влажности в здании, но их эмиссия непрерывна. Эмиссия органических химикалий из других материалов может быть в меньшей степени подвержена влиянию температуры и влажности, но большое влияние на их концентрацию в воздухе помещений будет оказывать вентиляция данных помещений.
Следует подчеркнуть, что каталитические эффекты для органических соединений очень велики. Так, скорость горения перхлората аммония с наиболее эффективным катализатором - оксинатом меди - при 300 ат превосходила скорость горения чистого перхлората в 21 раз. И даже при 1000 ат перхлорат с оксинатом меди горел в 4 раза быстрее чистого перхлората.
В табл. 25 суммированы полученные результаты и приведены значения В и V в уравнении горения. Заметим, что присутствие аммиака в молекуле органического соединения (салицилат аммония) не отражается на скорости горения - кривые для смесей перхлората аммония с салицилатом аммония и салициловой кислотой совпадают.
При полном сгорании большинства веществ образуются двуокись углерода, сернистый ангидрид и пары воды. При неполном сгорании образуются окись углерода, спирты, кетоны, альдегиды, кислоты и другие сложные органические соединения. Все они получаются в результате недостатка кислорода воздуха в зоне горения. Эти продукты способны гореть и могут образовать с воздухом взрывоопасные смеси, увеличивающие пожарную опасность. Кроме того, продукты неполного сгорания часто бывают едкими и ядовитыми, что затрудняет работу пожарных.
Соединения азота с точки зрения техники безопасности работы в химических лабораториях заслуживают особого внимания. Многие как неорганические, так и органические соединения его являются высокотоксичными, многие идут на получение взрывчатых веществ. Сам азот не обладает ни ядовитыми, ни раздражающими свойствами, он пассивен в процессе горения. Но при вдыхании больших концентраций его у человека появляются патологические явления, связанные с недостатком кислорода (кессонная болезнь). В то же время в различных формах своих соединений азот участвует в жизненно важных физиологических процессах. Наруше-, ния нормального течения азотного обмена в организме часто являются причиной тяжелых заболеваний. В лабораториях находят широкое применение следующие соединения азота азотная и азотистая кислоты, аммиак, хлористый нитрозил и др.
Как известно, все химические реакции подразделяются на гомогенные, протекающие в объеме, и гетерогенные, происходящие на поверхности раздела фаз. Процесс горения твердых материалов имеет гетерогенный характер. Поэтому исключительную роль в указанном процессе играют также размеры и природа поверхности твердой фазы и ее изменяемость. Для возникновения горения необходимы система, склонная к этому процессу (горючее вещество и окислитель), и импульс, вызывающий химическую реакцию горения. К горючему, способному взаимодействовать с окислителем, относятся значительное число жидкостей и газов, а также множество твердых веществ металлы в свободном виде, сера в элементарном и связанном виде, большинство органических соединений. Окислителями в процессах горения являются кислород (воздух), озон, перекиси, богатые кислородом вещества (нитросоединения, азотная кислота, перхлораты, нитраты), галогены.
Горение - это интенсивные химические окислительные реакции, которые сопровождаются выделением тепла и свечением. Горение возникает при наличии горючего вещества, окислителя и источника воспламенения. В качестве окислителей в процессе горения могут выступать кислород, азотная кислота, пероксид натрия, бертолетова соль, перхлораты, нитросоединения и др. В качестве горючего - многие органические соединения, сера, сероводород, колчедан, большинство металлов в свободном виде, оксид углерода, водород и т. д.
Большинство ВВ этой группы представляет собой кислородосодержащие органические соединения, способные к частичному или полному внутримолекулярному горению.
Хладоны в отличие от водо-пенных средств и инертных разбавителей являются ингибиторами горения, т. е. веществами, способными активно вмешиваться в химические процессы, тормозя их. Наиболее эффективно хладоны тормозят горение органических веществ (нефтепродуктов, растворителей и др.) и значительно слабее тормозят горение водорода, аммиака и некоторых других веществ. Хладоны неприемлемы для тушения металлов, многих металлоорганических соединений, некоторых гидридов металлов, а также тогда, когда окислителем при пожаре является не кислород, а другие вещества (например, галогены, оксиды азота).
Состав продуктов сгорания зависит от состава горящего вещества, условий, в которых происходит горение, и главным образом полноты сгорания-. В продуктах сгорания могут содержаться многие неорганические вещества (углерод, азот, водород, сера, фосфор и др.) и их окислы, а также спирты, кетоны, альдегиды и другие органические соединения. Образующийся в процессе горения дым состоит из мельчайших твердых частиц размером от 0,01 до 1 мкм.
Для неполярных органических соединений близок единице для слабополярных соединений можно приближенно принимать =1,06. Для пожаров нефтепродуктов, имеющих площадь горения более 10 м2, скорость выгорания (в м/с) приближенно можно найти по эмпирической формуле
Левая часть уравнений (6.2) и (6.3) выражает абсолютную энтальпию (внутреннюю энергию) исходной горючей смеси при начальной температуре Т0, а правая - энтальпию (внутреннюю энергию) смеси продуктов горения при температуре горения Тт или взрыва Гвзр. Детальная методика расчета температуры горения органических соединений, основанная на этих представлениях, описана в следующих двух разделах. При этом рассматриваются только системы, образованные углеродом, водородом, кислородом, азотом и аргоном, так как точный термодинамический расчет систем, содержащих другие элементы, без применения ЭВМ чрезвычайно сложен и выходит за рамки предлагаемой книги. Приближенные методы расчета малоэффективны, поэтому тоже не приводятся.
Острые и хронические отравления возможны также при розливе, фильтрации, очистке и транспортировке Hg при производстве гремучей ртути (при этом в воздух могут одновременно поступать окислы азота, эфиры азотной кислоты, пары летучих органических соединений, цианистый водород) прп извлечении благородных металлов из руд, сплавов, лома, отбросов при различных электролитических процессах при работах с фотореактивами, содержащими при различных химических процессах и операциях (например, в производстве синтетической уксусной кислоты в процессе анализа органических соединений при определении азота) при пропитке шпал, столбов и различных деревянных конструкций с целью их консервирования при использовании 1 как зонирующей (изолирующей) жидкости прп производстве электродов и электрических батарей при чистке, сварке илп ремонте котлов, в которых ранее содержалась при окраске подводных частей морских судов (Голдуотер и Джефферс) при контроле водомерных установок иногда - при пожарах на ртутных рудниках (Кулбасов Мирочник), при взрыве ртутных ламп, горении так называемых фараоновых змей (роданид ртути), взрыве гремучей ртути вблизи ртутных заводов при различных работах с Н, в частности в процессе изготовления ртутных колб (малых выпрямителей) и в производстве термометров.
Однако специфическое действие ингибирующих добавок ограничено. Наиболее эффективны галоидалканы, у которых большая часть атомов водорода заменена галоидом. Способные окисляться галоидопроизводные органических соединений, по-видимому, затрудняют горение только богатых горючим смесей. Добавление таких продуктов к бедным смесям может даже увеличивать скорость пламени вследствие возрастания при этом калорийности смеси.
В результате горения веществ образуются газообразные, жидкие и твердые продукты при полном сгорании получаются С02, Н20, ЯОз и Р205, не горящие и не поддерживающие горения вещества. При неполном сгорании органических веществ образуются более разнообразные продукты. В состав их, кроме продуктов полного сгорания, входят окись углерода, спирты, кетоны, альдегиды, кислоты и другие сложные органические соединения. Продукты неполного сгорания часто являются ядовитыми, способными гореть и образовывать с воздухом взрывчатые смесн. Продукты полного и неполного горения образуют различный по составу дым. Дым состоит из мельчайших твердых частиц, находящихся во взвешенном состоянии в каком-либо газе. Твердыми частицами являются главным образом углерод диаметром от 0,002 до 1 мм. Эти частицы легко оседают в виде копоти или сажи.
В результате горения образуются газообразные, жидкие и твердые продукты. При полном сгорании - СОг, НгО, БОг и Р2О5 при неполном сгорании образуются более разнообразные продукты, в состав которых, кроме продуктов полного сгорания, входят окись углерода, кетоны, альдегиды, кислоты и другие сложные органические соединения. Продукты неполного сгорания часто ядовиты, способны гореть и образовывать с воздухом взрывоопасные смеси.
Натрий Ыа, серебристо-белый мягкий металл. Ат. вес 22,997 плоти. 970 кг/м3, т. пл. 97,7° С т. кип. 883° С уд. электр. сопр. при 20° С 4,879 10" ом см. Теплота сгорания до Ыа202 2600 ккал/кг коэф. теплопроводности в кал/(см сек град) 0,317 при 21° С, 0,205 при 100° С. Обладает большой реакционной способностью. При нагревании на воздухе легко воспламеняется. Т. го-рёния около 900°С т. самовоспл. 330-360° С (в воздухе), 97-106°С (в присутствии перекиси натрия) II8°С (в кислороде) минимальное содержание кислорода, необходимое для горения, 5% объемн. скорость выгорания 0,7-0.9 кг/(м -мин). При сгорании в избытке кислорода образуется перекись Ыаг02, которая с легко-окисляющимися веществами (порошками алюминия, серой, углем и др.) реагирует очень энергично, иногда со взрывом. Твердая углекислота при соприкосновение с металлом, нагретым до 350°С, взрывается. Реакция с водой начинается при -98°С с выделением водорода. Взаимодействие натрия с водой, растворами кислот или органическими соединениями часто сопровождается взрывом. Натрий (особенно расплавленный) при горении образует взрывоопасные смеси с галоидпроизвод-ными углеводородами. Тушить составом ПС-1 и сжиженными инертными газами. При тушении в закрытых помещениях наибольший эффект дают аргон и азот. Тушение см. также Металлы. Средства тушения.
Пожароопасные свойства Горючий металл. Т. самовоспл. в воздухе 330-360°С (в присутствии пероксида натрия 97-106°С), в кислороде 118°С МВСК 5% об. скорость выгорания (1,1-1,5) I02 кг/(м3с). При сгорании в избытке кислорода образуется Na202, реагирующий с легкоокисляющимися веществами (порошками алюминия, серой, углем и др.), очень энергично, иногда со взрывом. Карбиды щелочных металлов обладают большой химической активностью в атмосфере диоксида углерода они самовоспламеняются, с водой взаимодействуют со взрывом. Твердый диоксид углерода с расплавленным натрием взрывается при 350°С. Реакция со льдом начинается при -98°С с выделением водорода. При соприкосновении значительных количеств натрия и воды реакция сопровождается взрывом. Взаимодействие с растворами кислот протекает подобно реакции с водой. Взаимодействие натрия с органическими соединениями зависит от их природы и температуры. Натрий, особенно расплавленный, при определенных условиях (например, при горении) образует взрывоопасные смеси с галоидопроизводными углеводородов. Азид натрия NaN3 взрывается при т-ре, близкой к т-ре плавления. В хлоре и фторе натрий воспламеняется при комнатной т-ре, с бромом взаимодействует при 200°С со взрывом. Вследствие повышенной химической активности натрий хранят под слоем керосина или минерального масла.
Атмосферные за1рязнения могут являться результатом практически любой операции, выполняемой при строительстве, техническом обслуживании или техническом ремонте кораблей и катеров. Загрязнители воздуха, которые контролируются во многих странах, включают в себя оксиды серы, оксиды азота, моноксиды углерода, микрочастицы (дым, сажа, пыль и т.д.), свинец и летучие органические соединения. При выполнении видов деятельности судостроения и судоремонта загрязнители включают в себя источники горения, такие как котельные и тепловые станции для обработки металла, генераторы и печи. Микрочастицы могут быть видимыми в качестве дыма от процесса горения, а также в качестве пыли при деревообработке, при операциях пескоструйной очистки, шлифовании песком, растирании и полировке.
Интересно отметить, что в интервале давлений 250-500 ат дигидрат бихромата меди(II) более эффективен, чем некоторые из рассмотренных выше органических соединений, что связано, вероятно, с лучшей растворимостью неорганических солей в воде, которая оказывает значительное влияние на процесс горения в этом диапазоне давлений. Органическая часть молекулы также оказывает весьма существенное влияние на каталитическую активность медьсодержащих соединений. Так, из табл. 20 и рис. 88 видно, что в зависимости от органической части молекулы коэффициент К может изменяться от 1,2 до 3,0 при 50 ат и от 10 до 21 при 300 ат, однако с ростом давления это различие становится меньше. При этом различие в каталитической эффективности, например, медьсодержащих органических соединений, не связано с абсолютным количеством металла в молекуле соединения. Так, в 5 вес.% салицилата меди содержится 0,96 г металла, а в оксинате меди - 0,83 г, тем не менее последнее соединение значительно более эффективно как катализатор. Аналогичная картина наблюдается и для натрийсодерямщих солей, например при 50 ат К - 1,3 для бензоата натрия, К = 1,8 для салицилата натрия и К = 0,7 для фуксина.
Что касается парадоксального уменьшения скорости горения перхлората аммония в присутствии некоторых органических соединений (см. табл. 20), особенно в области низких давлений, то оно связано, вероятно, с тем, что, поскольку ион данного металла (например, висмута, ртути, магния15 или кадмия) не оказывает каталитического воздействия на процесс, преобладающим является влияние органической части молекулы и, в частности, ее восстановительных свойств . Кроме того, не исключается участие иона металла в обменной реакции по типу, описанному ранее , и замедление горения вследствие связывания хлорной кислоты, продукты распада которой являются окислителем для горючих элементов перхлората.
Исходя из результатов таблицы, можно сделать вывод, что все изученные нами органические соединения ингибируют горение метана, но не в одинаковой мере. В зависимости от химической природы одни добавки имеют эффективность того же порядка, что и хлорид натрия (например, поливинилхлорид), другие - менее эффективны (о-фенилендиамин, бензоат лития, окись кремния), третьи - более эффективны (бензоат и сали-цилат натрия, индол, салицилат калия, дифтилметандисульфонат натрия).
Хотя многие из изученных нами органических соединений более эффективно чем хлорид натрия ингибировали распространение пламени в стехиометрической метано-воздушной смеси, однако следовало иметь в виду, что органические соединения могли принимать участие в процессе горения, переобогащая смесь. Для проверки этого предположения были поставлены опыты, когда в метано-воздушную смесь на бедном пределе горения (5% СН.) вводились изученные добавки. Результаты опытов представлены в табл. 58. Как видно из таблицы, твердые органические соединения, содержащие в молекуле щелочные металлы или хлор, а также соединения, содержащие аминогруппу, действительно являются ингибиторами.
Для каждого ВВ в определенной области давлений имеется свой наиболее эффективный катализатор горения - пятиокись ванадия, хромат свинца и хлорид меди для нитрогуанидина, дигидрат бихромата меди(II) я оксинат меди для перхлората аммония, соли шестивалентного хрома и хлориды, а также органические соединения щелочных металлов для литрата аммония.
В работе найдено, что окислы свинца реагируют с гидроксилпро-изводными углеводородов, горение которых они промотируют, и не реагируют с эфирами и углеводородами, горение которых они ингибируют. (Напомним, что промотирующее влияние гидроксила на каталитическое действие бихромата калия наблюдалось нами при горении пикриновой кислоты, что обусловлено, вероятно, его промотирующим влиянием на газофазное окисление СО.) В то же время органические соединения тетраэтилсвинец и пентакарбонилжелезо сильно ингибируют гексано-воздушные пламена , кроме того, они являются наилучшими антидетонаторами .
При горении ВВ соединения свинца и железа - эффективные катализаторы. Так, например, хромат и хлорид свинца катализировали горение нитрогуанидина и нитрата аммония, а органические соединения железа - эффективные катализаторы горения смееевых порохов на основе перхлората аммония. В то же время при термическом распаде этилнитра-та окись свинца была ингибитором, а медная поверхность ускоряла распад .
При полном сгорании органических соединений образуются С02, БОг, Н20, N2, а при сгорании неорганических соединений- оксиды. В зависимости от температуры плавления продукты реакции могут либо находиться в виде расплава (А1203, ТЮ2), либо подниматься в воздух в виде дыма (Р2О5, Ыа20,. А О). Расплавленные твердые частицы создают светимость пламени. При горении углеводородов сильная светимость пламени обеспечивается свечением частиц технического углерода, который образуется в больших количествах. Уменьшение содержания технического углерода в результате его окисления уменьшает светимость пламени, а снижение температуры затрудняет окисление технического углерода и приводит к образованию в пламени копоти.
Рассматривая любое органическое соединение как углеводород, в котором некоторое число атомов водорода замещено другими атомами и группами атомов и считая теплоту сгорания функцией числа электронов, перемещающихся при горении от атомов углерода и водорода к атомам кислорода, Карраш для жидких органических соединений пришел к зависимости
Хлористый водород как флегматизатор горения. Оксихлориро-вание углеводородов . В промышленности хлороорганического синтеза широко распространены системы, содержащие горючее, кислород и хлористый водород. Особенно часто встречаются такие смеси в процессах окислительного хлорирования (оксихлори-рования) . Основная задача этих процессов заключается в утилизации хлористого водорода, образующегося в качестве побочного продукта во многих производствах, прежде всего, в процессах прямого хлорирования органических соединений, а также дегидрохлорирования полихлоралканов. При прямом хлорировании насыщенных органических соединений основную брутто-реак-цию можно записать как
Горение – химический процесс соединения топлива с окислителем, сопровождающийся интенсивным тепловыделением и резким повышением температуры продуктов сгорания.
Горение сопровождается смесеобразованием, диффузией, воспламенением, теплообменом и другими процессами, протекающими в условиях тесной взаимосвязи.
Различают гомогенное и гетерогенное горение. При гомогенном горении тепло- и массообмен протекают между веществами, находящимися в одинаковом агрегатном состоянии (обычно газообразном).
Гетерогенное горение свойственно жидкому и твердому топливам.
Скорость химической реакции зависит от концентрации реагирующих веществ, температуры и давления и определяется произведением концентраций реагирующих веществ
где k 0 – эмпирическая константа.
Энергия активации E – это наименьшая энергия (для газовых смесей 85–170 МДж/кмоль), которой должны обладать молекулы в момент столкновения, чтобы быть способными к химическому взаимодействию. Разность энергий активации прямой и обратной реакции составляет тепловой эффект химической реакции.
Реакции характеризуются сильной экзотермичностью, обусловливающей рост температуры. Влияние температуры на скорость реакции значительно сильнее влияния концентрации реагирующих веществ. Поэтому, несмотря на уменьшение концентрации реагирующих веществ при горении, скорость реакции горения увеличивается и достигает максимума после выгорания 80–90% горючих веществ. Реакции горения газообразного топлива протекают практически мгновенно, что объясняется не только сильным влиянием температуры, но и цепным характером их протекания.
Скорость реакции зависит также от
давления
 (n
– порядок реакции).
(n
– порядок реакции).
Процесс горения топлива имеет две области: кинетическую, в которой скорость горения топлива определяется скоростью химической реакции, и диффузионную, в которой регулятором скорости выгорания является скорость смесеобразования. Примером кинетической области горения является горение однородной газовоздушной смеси. Диффузионно горит газообразное топливо, вводимое в реакционную камеру отдельно от окислителя.
Кинетическая область химического воздействия на скорость горения наиболее сильно ощущается при низких концентрациях, температурах и давлениях в смеси. В этих условиях химическая реакция может настолько замедлиться, что сама станет тормозить горение. Диффузионная область воздействия на скорость выгорания топлива проявляется при высоких концентрациях и температурах. Химическая реакция протекает очень быстро, и задержка в горении может быть вызвана недостаточно высокой скоростью смесеобразования.
Процесс смесеобразования практически не зависит от температуры.
Кинетическое горение готовой горючей смеси при турбулентном режиме движения очень неустойчиво. Поэтому в высокопроизводительных промышленных топочных устройствах при турбулентном режиме движения газовоздушных потоков горение является в основном диффузионным.
Процесс горения горючей смеси может начаться путем самовоспламенения или принудительного воспламенения (электрическая искра, факел и т.п.). Температура самовоспламенения определяется соотношением количества теплоты, выделяющегося при горении и отдаваемого во внешнюю среду. Количество теплоты, выделяющееся при горении, зависит от температуры и изменяется по экспоненте 1 (рис. 1.1)
где α – коэффициент теплоотдачи; A – площадь поверхности;T с - температура охлаждаемой стенки.
При небольшом отводе теплоты (прямая 2""" ) количество выделяемой теплотыq в >q от, поэтому реакция сопровождается повышением температуры системы, приводящим к самовоспламенению.
При большем отводе теплоты (прямая 2"" ) в точке Вq в =q от. ТемператураT в в этой точке называется температурой воспламенения горючей смеси. Она зависит от условий отвода теплоты и не является физико-химической константой, характеризующей данную горючую смесь. При увеличении отвода теплоты (прямая2" ) самовоспламенение невозможно. Точка А соответствует стабилизированному окислению в области низких температур, а точка Б – неустойчивому равновесию в области высоких температур.
Температура воспламенения может быть найдена из условий
q в =q от иdq в /dT =dq от /dT ,
определяемых точкой В (см. рис. 1.1).
С учетом уравнений (1.8) и (1.9) имеем
 .
Решив это уравнение, получим
.
Решив это уравнение, получим
|
|
Температура воспламенения T в для некоторых газов приведена в табл. 1.4.
Минимальная и максимальная концентрации горючей составляющей, ниже и выше которых не происходит принудительное воспламенение смеси, называются концентрационными пределами воспламенения (табл. 1.4); они зависят от количества и состава негорючих составляющих газообразного топлива, повышающих нижний и понижающих верхний пределы воспламенения.
 .
.